近日,圣湘生物自主研发的人乳头瘤病毒核酸检测试剂盒(PCR-荧光探针法)【以下简称“HPV13+2核酸检测试剂”】已正式获得国家宫颈癌筛查资质认证。圣湘生物成为国内第三家获得宫颈癌筛查资质产品的企业。
HPV13+2核酸检测试剂覆盖HPV16型、18型、31型、33型、35型、 39型、45型、51型、52型、53型、56型、58型、59型、66型和68型这15种型别的DNA并对16/18型进行分型,适用于宫颈癌初筛、联合筛查以及ASC-US人群分流。相较于WHO推荐的14种HPV高危型别,圣湘HPV13+2多出的53型是中国较为常见高危HPV基因型。研究数据显示,我国人群中HPV53型在高危型别中感染率占比近2.5%,本次圣湘生物HPV13+2核酸检测试剂是国内获得资质的产品中唯一一款覆盖15种HPV常见中高危型别的筛查产品,也是更适合中国人群的宫颈癌筛查产品。

自2017年起,圣湘生物开始启动多中心临床随访验证项目。该项目历时7年,在三大基层现场招募万名以上妇女参与研究,并进行为期三年的持续跟踪随访。通过前瞻性的大规模多中心临床试验验证以及超过一年的严格审评,圣湘HPV13+2核酸检测试剂最终获得了国家药监局的注册变更批件。
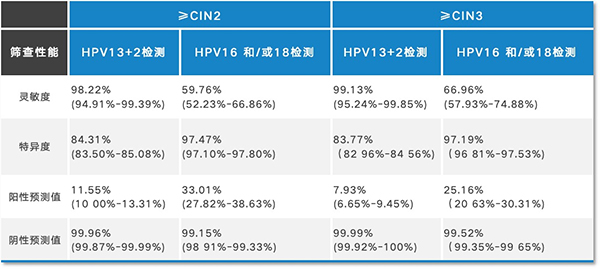
随访验证数据表明,圣湘生物HPV13+2核酸检测试剂在筛查性能方面表现出色,针对CIN2+的灵敏度达到98.22%,特异度为84.31%,阳性预测值为11.55%,阴性预测值高达99.96%。无论以CIN2+还是CIN3+作为临床终点,其灵敏度及阴性预测值均表现出较高水平,且临床灵敏度显著高于同类产品,能最大限度地筛查出可能的宫颈病变患者。
圣湘生物HPV13+2核酸检测试剂获批筛查资质,不仅有助于规范筛查产品的应用,提高各级卫生机构筛查能力及质量,而且能有效推动宫颈癌筛查项目高质量开展,全面促进全国各地落实加速消除宫颈癌行动计划,助力我国实现加速消除宫颈癌的目标。
圣湘生物积极响应国家政策,持续深耕妇儿健康领域,将围绕生殖健康方向,陆续推出生殖道感染、生殖内分泌、生殖遗传、宫颈癌甲基化产品、肠癌甲基化以及肠道感染等相关检测产品。同时,公司分子诊断、化学发光及测序等技术领域不断注入的强劲创新动力,也将持续助力生命科技普惠妇儿健康,普惠全球民众。

