11月25日,圣湘生物超敏肝炎核酸检测产品《乙型肝炎病毒核酸检测试剂盒(PCR-荧光法)》、《丙型肝炎病毒核酸检测试剂盒(PCR-荧光法)》获国家药品监督管理局批准上市,产品灵敏度分别达到国际一流水平的5IU/mL、12IU/mL,将全面助力全球2030年实现消除肝炎危害的目标。

圣湘生物肝炎核酸检测全面整体解决方案
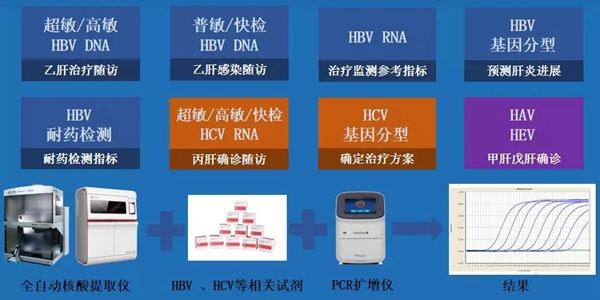
圣湘生物超敏肝炎核酸检测产品的上市,也标志着圣湘生物肝炎核酸检测全面整体解决方案的进一步完善,构建起了全面覆盖乙肝、丙肝、甲肝、戊肝等多种病毒性肝炎,全面覆盖病毒性肝炎筛查确诊、治疗方案确定、疗效评估、耐药监测、停药风险评估等全流程的齐全产品线,搭配公司一步法平台、磁珠法平台、仪器自动化提取平台和移动分子诊断(POCT)平台,能够提供适合不同医疗机构、不同应用场景,满足不同阶段、不同层级临床需求的全面整体解决方案。
全球肝炎感染现状严峻
据统计,全球约有3.25亿人感染慢性乙型肝炎病毒(HBV)和丙型肝炎病毒(HCV)。其中HBV感染约2.57亿,HCV感染约7100万。中国有慢性乙肝感染者8600万,慢性乙肝患者2000~3000万,肝硬化肝癌患者700万;丙肝感染者超过1000万。
目前我国乙肝、丙肝的诊断率分别为19%、17.7%,治疗率分别为11%、1.3%,和世界平均水平相差较大,实现世界卫生组织(WHO)提出的2030消除肝炎危害目标(2030年乙肝、丙肝诊断率要达到90%,治疗率要达到80%)任务较为艰巨。
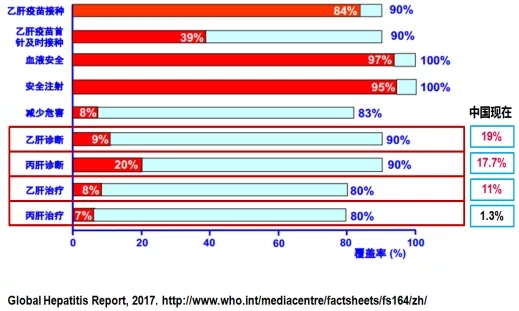
红色:世界平均水平 浅蓝:2030目标
高灵敏度肝炎核酸检测意义重大

超敏HBV DNA检测不仅是慢乙肝抗病毒治疗期间的抗病毒治疗适应证选择及疗效判断的重要指标,还在隐匿性乙肝病毒感染(OBI)筛查、术前检查、肿瘤患者放化疗后HBV再激活风险评估、抗病毒治疗疗效与终点评价以及预测HBeAg阴性患者HBV耐药突变等方面表现出了突出的临床价值。
超敏HCV RNA检测不仅用于HCV现症感染的确认、抗病毒治疗前基线病毒载量分析,以及抗病毒治疗过程中及治疗结束后的应答评估,还对丙肝患者接受透析治疗期间的监测、术前检查等方面有明确的临床意义。
圣湘生物独有专利技术
实现超灵敏检测
1、专利磁珠修饰技术:专用的基质磁珠,偶联核酸亲和基团,增强核酸捕获。
2、纳米核壳技术:纳米级别磁性核心+分子聚合物外壳,表面比最大化,保证核酸富集空间。
3、内标专利技术:参与提取和扩增全过程,预防假阴性,确保结果准确,防止漏检。
4、先进的酶修饰技术:经过特定修饰的酶,活性更高,对干扰物耐受更强。
其中乙型肝炎病毒核酸检测试剂盒,线性范围2.0E+01~2.0E+09IU/mL,最低检出限达到5IU/mL;丙型肝炎病毒核酸检测试剂盒,线性范围为2.5E+01~1.0E+08IU/mL,最低检出限达到12IU/mL。
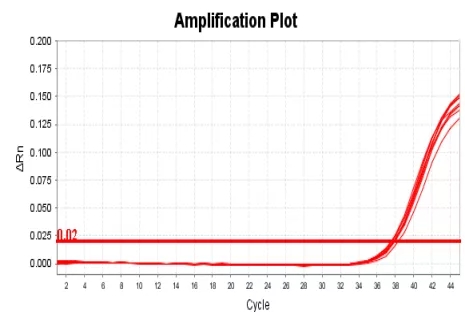
乙肝5IU/mL检测图
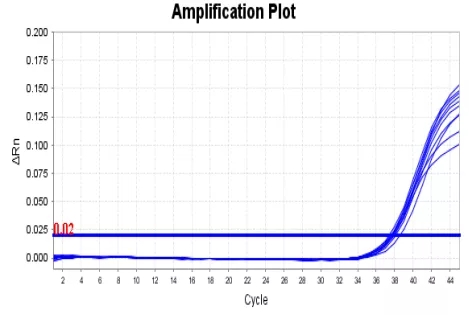
丙肝12IU/mL检测图
肝炎核酸检测项目EQA参评客户数
圣湘生物位居行业第一
依托于圣湘生物肝炎检测全面整体解决方案优势,在每年国家卫健委临检中心开展的全国 PCR 测定(病毒学)室间质量评价(EQA)活动中,使用圣湘生物肝炎核酸检测产品的参评客户数大幅增长。2019年,圣湘生物乙肝核酸检测项目参评客户数达到行业第一,丙肝核酸检测项目参评客户数直逼行业第一。
2013-2019年主要厂家
乙肝核酸检测项目EQA参评客户数
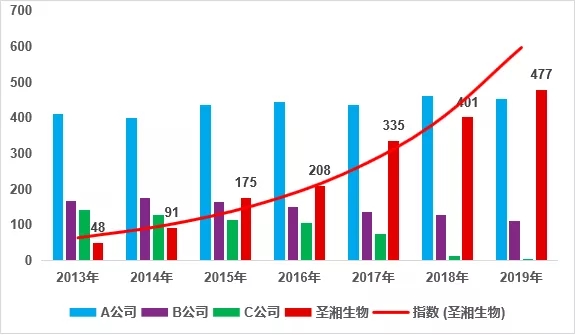
2013-2019年主要厂家
丙肝核酸检测项目EQA参评客户数
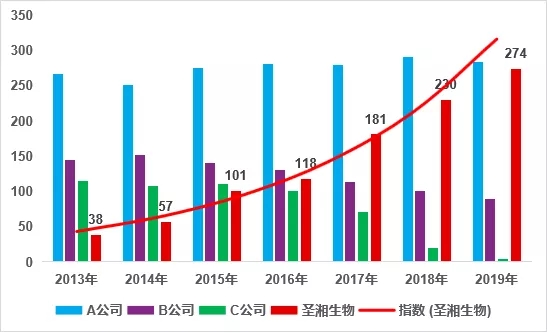
数据来源:国家卫健委临检中心
感谢各位专家、广大客户的信任和支持,未来,圣湘生物将在肝炎检测领域继续深耕,推出更多满足临床需求的高性能产品。消灭肝炎,永不止步!

